 Ihmisen elon alkuperä on ikuinen kysymys, eikä ihmiskunta ei ole kyennyt muodostamaan yhteistä näkemystä siitä, missä vaiheessa tai millaisissa soluissa elämä alkaa.
Ihmisen elon alkuperä on ikuinen kysymys, eikä ihmiskunta ei ole kyennyt muodostamaan yhteistä näkemystä siitä, missä vaiheessa tai millaisissa soluissa elämä alkaa.
Lähes aina kyse on kuitenkin hedelmöittymiseen tai raskauteen liittyvistä määritelmistä, mutta kaksi maaliskuussa 2021 Naturessa julkaistua tutkimusta (1,2) vievät meidät kysymään, voiko jossain tapauksessa tavallisista ihosoluista syntyä uusi ihminen.
Ihmettelisin, jos asiasta ei nousisi jonkun sortin eettistä debattia, sen verran uusille rajoille asiassa mennään.
Perinnöllisyyslääkärin ja kantasolututkijan elämään kuuluu yllättävän tiuhaan pohdintaa siitä, miten mihinkin pitäisi suhtautua. Usein tällaiset geeni- ja solumaailman kysymykset nousevat yllättäen, mikä johtunee tutkimuksen ja (bio)tekniikan etenemisen suuresta vauhdista. Uutta tietoa tulee sellaisella nopeudella, että asioihin perehtyneenkin on vaikea aina sijoittaa kaikkia osasia paikoilleen.
”Elämän” alku ilman hedelmöittymistä, viljelyolosuhteita muuttamalla
Koronamaailman keskellä tutkijat ovat siis jatkaneet elämän alkuvaiheiden selvittelyä, ja näistä tutkimuksissa on saatu mielenkiintoisia löydöksiä. Tällä kertaa tutkimuksissa kuvataan uusi, hyvin varhaisen ihmiselämän kaltainen rakenne, joka on syntynyt ilman hedelmöittymistä, munasolua tai siittiötä.
Tällainen ”elämän” alku on siis, mikäli mahdollista, entistäkin vaikeampi määrittää, kun se saadaan aikaan vain viljelyolosuhteita muuttamalla. Juuri nyt emme siis tiedä, onko kyseessä edes potentiaalinen ihmiselämä. Toistaiseksi lienee turvallisempaa puhua vain solujen muodostelmasta, joka tosin on hyvin samanlainen kuin ihmisen alkio.
Yksilönkehityksen ensimmäisillä vaiheilla on suuri merkitys muun muassa varhaisten keskenmenojen synnylle, ja tutkimuksen tavoitteena oli niiden ymmärtäminen. Tiedon hankkimista varten kehitettiin viljelymenetelmiä, jotka mallinsivatkin hyvin ihmisen varhaista alkiota.
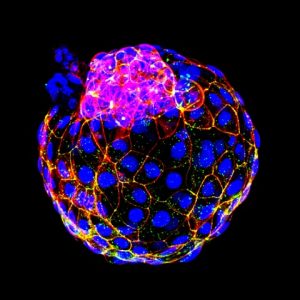
Kehittyneitä solumuodostelmia kutsutaan artikkeleissa ”blastoideiksi” tai ”iblastoideiksi”, koska ne muistuttavat niin läheisesti noin viikon sisällä hedelmöittymisestä muodostuvaa alkiorakkulaa, blastokystia. Suuri ero oikeaan alkioon on kuitenkin se, että kahden yhtyneen sukusolun sijaan blastoidi voidaan saada aikaan vaikka aikuisen ihmisen ihosta, indusoimalla pintakerroksen fibroblasteja soluviljelmässä monikykyisten kantasolujen suuntaan.
Toisen ryhmän tutkimuksessa liikkeelle lähdettiin vuosikausia vanhasta tutkimusmallista eli WIBR3-nimisestä monikykyisestä alkion kantasolulinjasta, joten siinäkään ei käytetty yksilönmuodostukseen kykeneviä alkioita.
Molempien ryhmien tulokset ovat hyvin samankaltaisia. Tutkimuksissa huomattiin, että ihmisen solujen viljeleminen tietyissä olosuhteissa sai aikaan kaikkia alkion syntyyn vaadittavia soluja. Pallomaiseen kudokseen syntyi alkion sisäsolumassaa vastaava rakenne ja kaikkien kolmen alkiokerroksen soluja.
Varsinaista alkiota rakentavien solujen lisäksi blastoidiin syntyi myös kehityksessä tarvittavia alkion ulkoisia soluja, kuten sikiökalvoja muodostavia hypoblastisoluja sekä ulkokerroksen trofoblasteja, joista syntyy istukka. Kummassakaan tutkimuksessa blastoideja ei kasvatettu pitkiä aikoja, koska tavoitteena oli siis tutkia, mitä varhaisessa alkiossa tapahtuu blastokystin muotoutuessa.
Molemmat ryhmät ilmoittivat myös haluavansa tulkita kansainvälisiä tutkimusohjeita tiukimman mukaan ja kohtelivat tämän vuoksi blastoideja samoin kuin oikeita blastokysteja. Kantasolututkimuksen ohjeet ja muun muassa Suomen lainsäädäntö kieltävät kasvattamasta oikeita ihmisalkioita yli 14 vuorokauden ajan hedelmöityksestä (3).
Kuinka blastoideihin pitäisi suhtautua?
Onko kyseessä pienen pieni ihmisen alkio, jolla olisi potentiaalia kasvaa oikeaksi yksilöksi? Haluammeko edes tietää, vai joudummeko asiassa vain syvemmälle suohon? Niin sanottua synteettisten alkioiden tutkimusta ja etiikkaa on pohdittu aiemminkin (4), ja yksi periaatteista on, että tällaisia alkioita ei tule käyttää raskauden aikaansaamiseksi.
Useimmat keskustelijat tuntuvat nyt ajattelevan, että blastoidit ovat tutkijoille tervetullut keino hankkia tietoa ihmisen alkion varhaisista solutapahtumista, joita voidaan tutkia ilman, että siihen käytetään oikeita alkioita.
Voi kuitenkin olla, että mielipiteet tästä vielä muuttuvat, ja on kieltämättä häkellyttävä ajatus, että aikuisen soluista saataisiin aikaiseksi todella kehittymiskykyinen alkio vain geenien ilmentymistä ja viljelyolosuhteita muuttamalla. Mikäli näin on, pidän lähes varmana, että tällaisten kloonattujen alkioiden käyttöä tullaan sääntelemään tiukasti. On kokonaan toinen asia, voidaanko sääntelyä valvoa tai käyttöä estää.
Joka tapauksessa kyseessä on mielestäni taas yksi hyvä esimerkki siitä, kuinka tiede osoittaa jälleen, mitä kaikkea emme tiedä ja minkälaisista asioista emme ole vielä edes osanneet olla eri mieltä. Harvan mieleen on juolahtanut, että ihonpalasta voitaisiin kasvattaa koko alkio!
Kirmo Wartiovaara
dosentti, Helsingin yliopisto, perinnöllisyyslääkäri, HUS
Viitteet:
1) Yu, L., Wei, Y., Duan, J. et al. Blastocyst-like structures generated from human pluripotent stem cells. Nature (2021). https://doi.org/10.1038/s41586-021-03356-y
2) Liu, X., Tan, J.P., Schröder, J. et al. Modelling human blastocysts by reprogramming fibroblasts into iBlastoids. Nature (2021). https://doi.org/10.1038/s41586-021-03372-y
3) Laki lääketieteellisistä tutkimuksista (§13), https://finlex.fi/fi/laki/ajantasa/1999/19990488#L3P13
4) Rivron N ym. Debate ethics of embryo models from stem cells. Nature 564, 183-185 (2018)


 Sillä, mitä suuhun panemme, on tunnetusti suuri vaikutus terveyteen – ajatellaanpa nyt esimerkiksi ravitsemuksen suhdetta sydän- ja verisuonisairauksiin, diabetekseen ja syöpätauteihin. Eikä silloin puhuta vain ehkäisystä, vaan myös hoidosta. Monien mielestä ravitsemusoppia opetetaankin aivan liian vähän lääkäreille.
Sillä, mitä suuhun panemme, on tunnetusti suuri vaikutus terveyteen – ajatellaanpa nyt esimerkiksi ravitsemuksen suhdetta sydän- ja verisuonisairauksiin, diabetekseen ja syöpätauteihin. Eikä silloin puhuta vain ehkäisystä, vaan myös hoidosta. Monien mielestä ravitsemusoppia opetetaankin aivan liian vähän lääkäreille.
 Etelä-Suomen talvilomaviikko ja koko maa tursuaa lunta. Mikä helpotus – vai peräti unelmien täyttymys – koronakurjimuksen keskellä kaikille matkustusrajoituksista kärsiville.
Etelä-Suomen talvilomaviikko ja koko maa tursuaa lunta. Mikä helpotus – vai peräti unelmien täyttymys – koronakurjimuksen keskellä kaikille matkustusrajoituksista kärsiville.